
年付专属活动专区,提供多地区云服务器产品,年付价格更具性价比,适合长期稳定业务使用。


















































携手合作伙伴,实现业务上的双向合作共赢
我们为您提供全方位的支持与服务,确保您在使用我们的云服务时无忧无虑。
10+年商誉沉淀,深耕中国香港及海外高端资源
一、引言
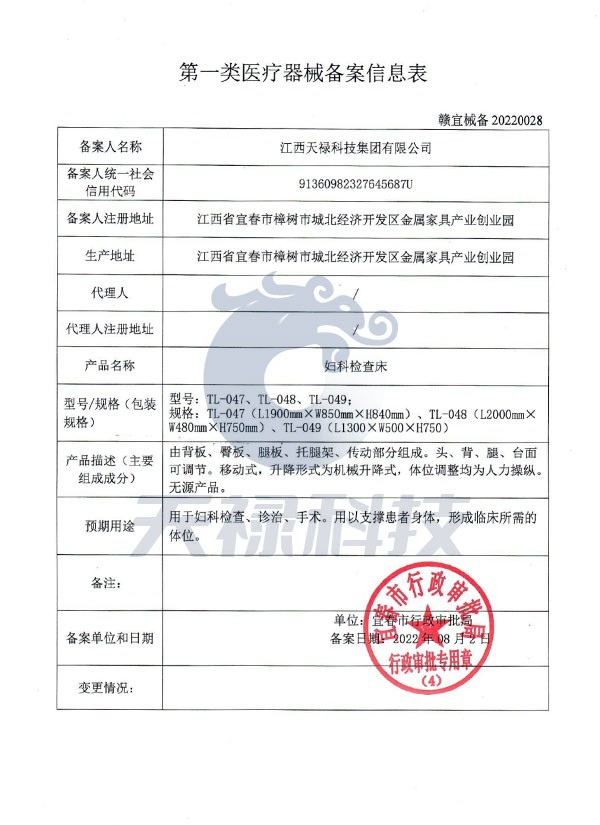
医疗器械是医疗领域不可或缺的重要设备,为确保境内使用的医疗器械的安全性和有效性,本文将详细阐述境内第一类医疗器械备案清理规范,以确保医疗器械从生产到使用全过程的安全可控。

二、备案流程概述
备案流程主要包括以下几个步骤:申请与提交材料、审查与批准、发放备案凭证等。在这一过程中,涉及到的材料主要包括产品技术参数、企业资质证明等文件。申请方需要严格按照相关规定,完整准确地提交相关材料。
三、清理规范内容
针对境内第一类医疗器械备案的清理规范主要包括以下几个方面:
四、具体实施方案
为确保清理规范的有效实施,可采取以下措施:
五、总结
境内第一类医疗器械备案清理规范是保障医疗器械安全使用的关键环节。通过加强备案流程的监管和清理规范,可以有效保障人民群众的健康和安全。因此,各方应严格遵守相关规定,共同推动医疗器械行业的健康发展。
高速稳定云服务器9.9元起

